
安进(Amgen)近日在第18届偏头痛信托国际研讨会(MTIS 2020)上公布了评估偏头痛药物Aimovig(erenumab)治疗发作性偏头痛(episodic migraine,EM)成人患者一项2期研究(NCT01952574)5年开放标签治疗期(OLTP)的长期安全性和疗效数据。结果显示,Aimovig不仅帮助患者持续减少了每月偏头痛天数,而且还减少了急性偏头痛特异性药物(AMSM,如曲普坦[triptans])的使用。此外,安全性与该研究的双盲治疗期观察到的结果一致,5年暴露期间不良事件发生率没有增加。这些5年数据进一步增加了Aimovig对偏头痛患者的既定益处。
Aimovig是全球批准的首个靶向降钙素相关基因肽(CGRP)靶点的偏头痛药物,该药由诺华和安进在美国共同商业化。安进拥有在日本市场的独家商业化权利,诺华拥有世界其他地区的独家商业化权利。
会上公布的这些额外的长期数据补充了Aimovig作为最常用的抗CGRP药物的地位。自上市以来,在全球范围内已有超过44万例患者被处方了Aimovig治疗。
这项OLTP研究(NCT01952574)评估了Aimovig 70mg和140mg治疗EM(试验中定义为:基线时每月偏头痛发作天数4-14天、头痛天数<15天)的持续疗效和长期安全性。在完成了为期12周的随机、双盲、安慰剂对照期(DBTP)后,383例符合资格的EM成人患者进入开放标签治疗期(OLTP)。所有患者在最初每月接受70mg剂量Aimovig,在修订方案以评估更高剂量的长期安全性之后,共有250例患者将剂量从70mg提高至140mg。疗效终点包括每月偏头痛天数(MMD)和急性偏头痛特异性药物(AMSM)治疗天数相对基线的变化。安全性和耐受性通过监测不良事件、心电图、实验室评估和生命体征来评估。
数据显示,在完成开放标签治疗期(OLTP)的216例患者中,平均每月MMD从DBTP基线8.7天减少了5.3天。到研究结束时,使用AMSM治疗偏头痛的患者,平均每月AMSM使用天数从DBTP基线6.2天减少了4.4天。与DBTP相比,使用Aimovig治疗5年期间没有观察到新的安全信号或不良事件发生率增加。Aimovig的安全性和耐受性与其他临床试验数据一致,最常见的副作用是鼻咽炎、上呼吸道感染和流感。
在MTIS 2020会议上,安进还公布了Aimovig其他研究的数据,包括LIBERTY开放标签扩展研究的中期结果,以及Aimovig在EMPOwER研究中的有效性和安全性结果。这些研究加强了Aimovig对不同背景的发作性偏头痛(EM)患者的安全性和有效性。
LIBERTY研究(NCT03096834)的开放标签扩展研究的中期2年结果显示,在先前接受过2-4种预防性疗法治疗失败的EM患者中,Aimovig显示出持续的疗效、不良事件发生率没有增加。3期EMPOwER研究(NCT03333109)的结果强调了Aimovig对来自亚洲、中东和拉丁美洲的EM成人患者的有效性和安全性。
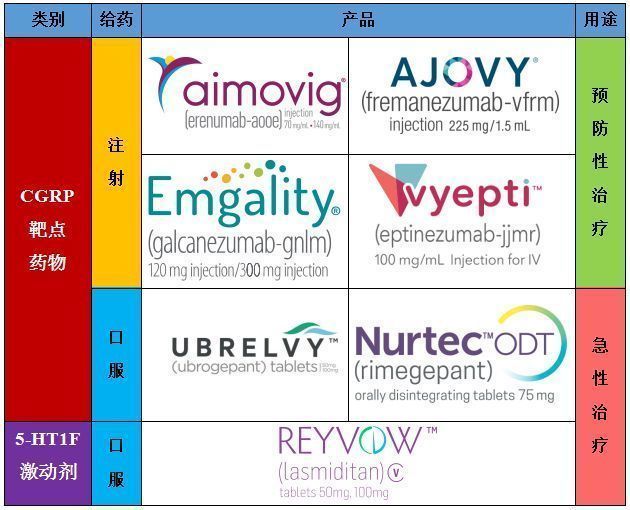
降钙素相关基因肽(CGRP)是一种神经肽,已被证明在偏头痛发作时释放,被认为是偏头痛发作的诱因。目前,CGRP及其受体已成为偏头痛药物研发的热门靶点。
截至目前,已有4款以CGRP及其受体为靶点的单抗类偏头痛疗法上市,除了Vyepti之外,另外三款分别为:安进/诺华Aimovig(靶向CGRP受体)、梯瓦Ajovy(靶向CGRP)、礼来Emgality(靶向CGRP)。用药方面,Vyepti每3个月一次静脉输注,Aimovig和Emgality均为每月一次皮下注射,Ajovy则可每月一次或每3个月一次皮下注射。
另有一些药企正在开发口服CGRP受体拮抗剂。目前已上市的有艾尔建的Ubrelvy(ubrogepant)和Biohaven公司的Zydis ODT(rimegepant口腔崩解片),2款药物用于成人偏头痛(有或无先兆)急性治疗。特别值得一提的是,2019年10月,礼来口服药物Reyvow(lasmiditan)获得美国FDA批准用于成人偏头痛(伴或不伴先兆症状)急性治疗。该药是一种5-HT1F激动剂,是20年来批准的首个新一类急性偏头痛治疗药物。
原标题:偏头痛药物!安进公布5年开放标签研究:证实Aimovig治疗发作性偏头痛具有长期疗效和安全性!







